Protein S-Mangel, hereditär
Ein Mangel an aktivem Protein S führt zu einer verminderten antikoagulatorischen Aktivität und einer erhöhten Disposition für Thrombosen. Ursächlich sind pathogene Varianten im PROS1-Gen, die in homozygoter oder kombinierter heterozygoter einen Protein S-Mangel-Mangel bedingen.
Wissenschaftlicher Hintergrund
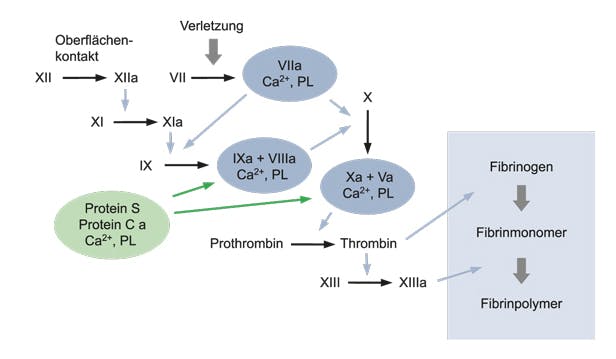
Ein Mangel an aktivem Protein S (Protein S-Aktivität <60%) führt zu einer verminderten antikoagulatorischen Aktivität. Protein S ist ein Vitamin K-abhängiges Protein, welches als Kofaktor des aktivierten Protein C die Inaktivierung der Gerinnungsfaktoren Va und VIIIa beschleunigt. Normalerweise liegen ca. 60% von Protein S im Komplex mit dem C4b-Bindeprotein vor, und nur freies Protein S steht dem aktivierten Protein C als Kofaktor zur Verfügung.
Protein S-Mangel ist mit einer erhöhten Neigung zu venösen Thrombosen vom 1. – 4. Lebensjahrzehnt an verbunden.
Der angeborene Protein S-Mangel wird wie folgt klassifiziert:
- Typ I: Quantitativer Defekt, Verminderung von gesamtem und freiem Protein S sowie der Protein S-Aktivität
- Typ II: Qualitativer Defekt, verminderte Protein S-Aktivität bei normaler Konzentration an freiem und gesamtem Protein S
- Typ III: Quantitativer Defekt, freies Protein S und Protein S-Aktivität vermindert bei normaler Plasma-Konzentration von gesamtem Protein S
Die Ausprägung des klinischen Phänotyps und das Erkrankungsalter werden durch Art und Lokalisation von Varianten im PROS1-Gen beeinflusst. Sehr selten ist der homozygote oder kombiniert heterozygote Protein S-Mangel, der häufig zu perinataler Purpura fulminans oder massiven Thrombosen mit letalem Ausgang führt. In der Regel weisen diese Patienten eine Protein S-Aktivität von <5 % auf. Wichtig ist die Abgrenzung zum erworbenen Protein S-Mangel, der häufig im Zusammenhang mit Entzündung, Sepsis, Verbrennung, Polytrauma, Vitamin K-Mangel oder großen Operationen auftritt. Die Einnahme von Ovulationshemmern senkt ebenfalls die Protein S-Aktivität, so dass in diesen Fällen die untere Grenze des Normbereichs für die Protein S-Aktivität bei 50 % liegt. Mit der molekulargenetischen Untersuchung können bei über 60 % der Patienten mit Verdacht auf einen angeborenen Protein S-Mangel ursächliche Varianten nachgewiesen werden. Dies entspricht 1-2 % aller Patienten mit tiefen Venenthrombosen. Größere Deletionen einzelner Exons oder häufiger des gesamten Gens machen ca. 2-5 % aller Varianten aus. Diese können mittels MLPA analysiert werden.
Erkrankung | ICD—10 | Gen | OMIM—G |
| Protein-S-Mangel | I82.9 | PROS1 | - |
Alhenc-Gelas et al. 2016, Thromb Haemost. 115:570 / Klostermeier et al. 2015, Thromb Haemost 113:426 / Duebgen et al. 2012, Am J Clin Pathol / Pintao et al. 2010, Hum Genet 127:121 / ten Kate et al. 2008, Hum Mutat 29:939 / Yin et al. 2007, Throm Haemost 98:783 / ten Kate et al 2006, Haematologica 91:1151
letzte Aktualisierung: 10.4.2024